Trong Hóa học, liên kết cộng hóa trị là một liên kết cơ bản thường gặp. Tuy nhiên không phải ai cũng hiểu rõ khái niệm này và các đặc điểm của nó. Hãy cùng LabVIETCHEM tìm lời giải đáp qua bài viết sau nhé!
1. Liên kết cộng hóa trị là liên kết gì?
Liên kết cộng hóa trị (LKCHT) được tạo thành bởi 2 loại nguyên tử bằng một hay nhiều cặp electron dùng chung. Cũng có thể hiểu đó là liên kết giữa 2 ion hay 2 nguyên tử có các cặp electron chia sẻ cho nhau.
Theo đó mỗi cặp electron được chia sẻ giữa 2 nguyên tử và gọi là cặp liên kết. Nếu không được chia sẻ thì sẽ gọi là cặp đơn độc. Một số phân tử dùng chung electron sẽ khiến nguyên tử đạt được nhiều cấu hình electron bền vững.
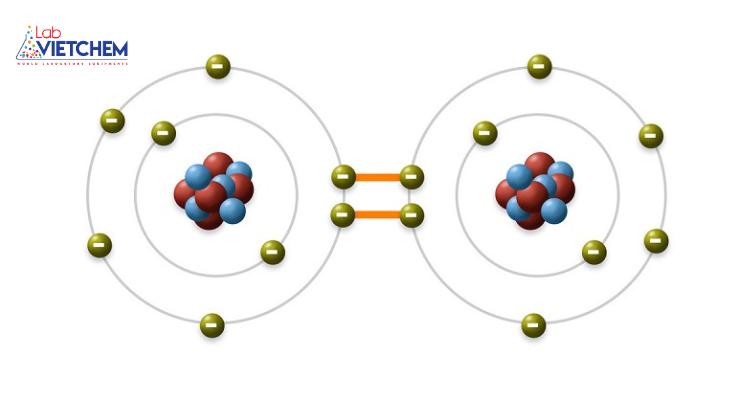
Hình 1: Liên kết cộng hóa trị
2. Phân loại các liên kết cộng hóa trị
2.1. Liên kết cộng hóa trị phân cực
LKCHT phân cực hình thành khi các electron dùng chung giữa các nguyên tử không chia sẻ đều nhau. Nguyên nhân là vì một phía nguyên tử có độ âm điện cao hơn so với phía còn lại (tương đương với lực hút lớn hơn).
Do đó phân tử sẽ nghiêng về bên chứa nguyên tử có độ âm điện thấp hơn, và phía hơi âm chứa nguyên tử có độ âm điện cao hơn. Kết quả tạo ra hợp chất cộng hóa trị sẽ có một thế tĩnh điện.
2.2. Liên kết cộng hóa trị không phân cực
LKCHT không phân cực hình thành khi các nguyên tử chia sẻ electron đồng đều nhau. Nghĩa là cả hai nguyên tử đều cùng điện từ hoặc có lực tương tự nhau. Theo đó sức hút sẽ càng mạnh nếu giá trị lực điện tử của chúng càng gần nhau.
Mặt khác, điều này cũng xảy ra trong các phân tử khí (diatomic). Hạt có độ âm điện cao sẽ hút các electron ra khỏi bên yếu hơn.
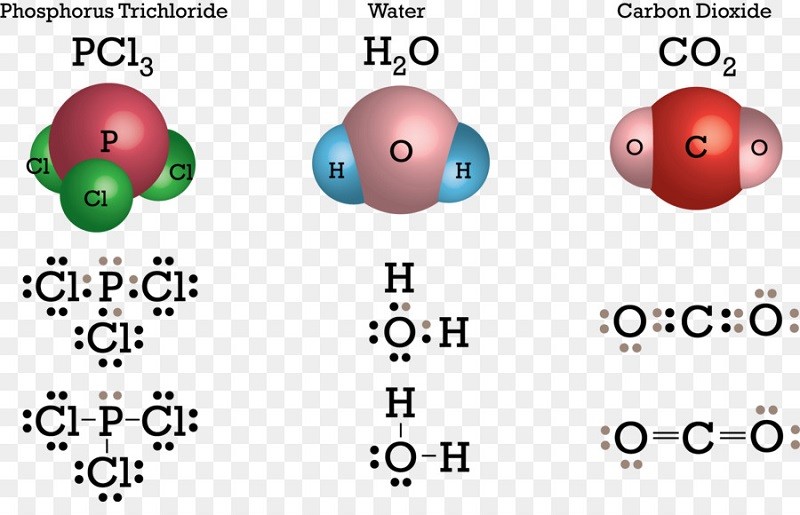
Hình 2: Liên kết cộng hóa trị không phân cực
2.3. Liên kết đơn phân tử
Liên kết này diễn ra khi 2 phân tử chỉ chia sẻ 1 cặp electron. So với các liên đôi và liên kết ba, thì liên kết đơn yếu hơn và có mật độ nhỏ hơn. Thế nhưng nó lại là liên kết ổn định nhất trong các liên kết.
Bởi vì mức độ phản ứng của liên kết thấp nên khi bị mất electron sẽ không bị ảnh hưởng nhiều.
2.4. Liên kết đôi phân tử
Nếu liên kết đơn 2 phân tử chỉ chia sẻ 1 cặp electron thì ở liên kết đôi sẽ là 2 cặp electron.
Liên kết này được thể hiện bằng hai đường gạch ngang (-) nằm giữa hai nguyên tử trong một phân tử. Mặc dù mạnh hơn liên kết đơn nhưng liên kết đôi lại kém ổn định hơn.
2.5. Liên kết ba phân tử
Liên kết ba phân tử là liên kết cộng hóa trị kém ổn định nhất. Liên kết này diễn ra khi có 3 cặp electron được chia sẻ giữa hai nguyên tử của một phân tử.
3. Đặc điểm của liên kết cộng hóa trị
Liên kết cộng hóa trị có những đặc điểm nổi bật sau:
3.1. Dạng tồn tại
Phân tử có LKCHT có thể tồn tại ở trạng thái chất rắn như: đường, sắt, lưu huỳnh… hay ở chất lỏng như: rượu, nước…còn ở trạng thái chất khí là: hidro, clo, cacbonic…
Thường các chất này có điểm sôi và độ nóng chảy thấp, đồng thời có entanpi hóa hơi và nhiệt hạch thấp.
3.2. Những chất có cực
Những chất có cực như: đường, ancol etylic... sẽ tan nhiều trong môi trường dung môi có cực như nước.
3.3. Những chất không cực
Những chất không cực như ion, lưu huỳnh… sẽ tan trong các dung môi không cực như: benzen, cacbon tetraclorura…
Chất chỉ có liên kết cộng hóa trị không cực không có khả năng dẫn điện ở mọi trạng thái.
4. Cách nhận biết liên kết cộng hóa trị và liên kết ion
4.1. Đặc điểm liên kết ion
- Liên kết ion được tạo ra giữa 2 nguyên tử khác nhau, trong đó một nguyên tử sẽ nhường electron cho một nguyên tử khác.
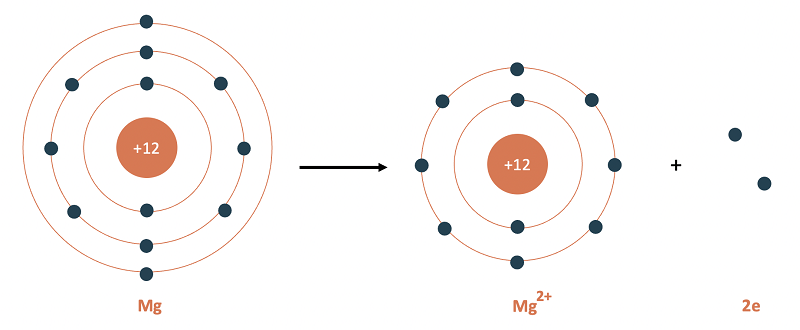
Cho nhận e của nguyên tử Mg
- Vì mỗi nguyên tử đều có ít hơn một electron và nguyên tử kia lại có thêm một nguyên tử, nên hai nguyên tử này đều trở thành các ion.
- Ion kim loại bị mất một electron sẽ có điện tích dương và ion phi kim loại thu được một electron có điện tích âm. Điều này dẫn đến các ion sẽ hút mạnh vào nhau để tạo nên liên kết.
- Các hợp chất ion thường sẽ ở dạng rắn như muối. Nhờ vào điểm nóng chảy cao khi hòa tan vào nước mà tạo ra độ dẫn điện cao.
4.2. Đặc điểm liên kết cộng hóa trị
- LKCHT xuất hiện khi nguyên tử có một electron nằm ở lớp vỏ ngoài và một nguyên tử khác cần một electron để lấp đầy lớp vỏ ngoài.
- Khi đó hai nguyên tử này sẽ kết hợp lại để cùng chia sẻ electron. Kết quả cả hai nguyên tử đều có vỏ ngoài đầy đủ và có cấu hình điện tử ổn định.
- Đối với liên kết cộng hóa trị, nếu nguyên tử kim loại có một electron nằm ở lớp vỏ ngoài và phi kim cần một electron để lấp đầy. Thì nguyên tử kim loại và nguyên tử phi kim sẽ chia sẻ electron đồng đều nhau.
Trên đây là toàn bộ thông tin về liên kết cộng hóa trị do LabVIETCHEM tổng hợp và chia sẻ. Hi vọng bài viết đã cung cấp nhiều kiến thức hữu ích giúp bạn vận dụng tốt vào công việc và học tập.
Nếu còn điều gì thắc mắc và muốn được giải đáp, hãy liên hệ ngay với chúng tôi nhé!



